Gesundheitsversorgung Arzneimittel: Eine Übersicht
Arzneimittel (Medikamente) werden zur Verhütung, Behandlung, Linderung oder Diagnose von Erkrankungen eingesetzt. Neben Medikamenten mit chemisch hergestellten Wirkstoffen gibt es auch Medikamente, deren Wirkstoffe aus biologischen Materialien gewonnen werden.
Auf einen Blick
- Arzneimittel können vorbeugend, heilend oder lindernd wirken oder als Diagnosemittel eingesetzt werden.
- Die meisten Arzneimittel bekommt man nur in Apotheken, viele sogar nur mit einem Rezept.
- Die Wirkstoffe können nicht nur chemisch hergestellt werden, sondern auch aus menschlichem oder tierischem Material (Biologika) oder aus Pflanzen gewonnen werden (pflanzliche Arzneimittel).
- Generika und Biosimilars ahmen Präparate nach Ablauf des Patentschutzes nach. Sie sind wirkungsgleich, aber kostengünstiger als das Originalpräparat.
- Bevor ein Arzneimittel auf den Markt kommt, muss es in der Regel geprüft und zugelassen werden. Manchmal ist eine Registrierung ausreichend.
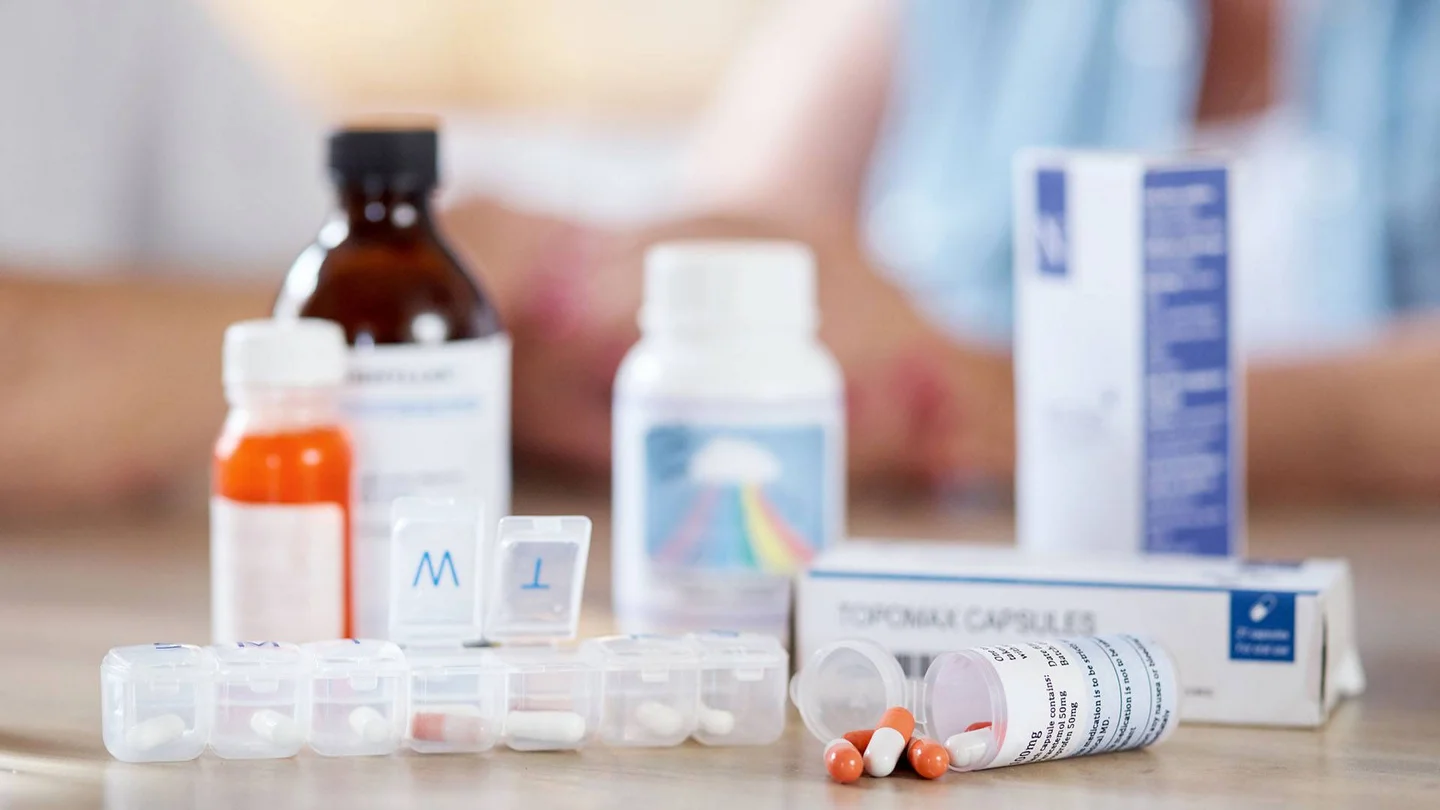
Was sind Arzneimittel?
Arzneimittel oder Medikamente sind Produkte, die zur Behandlung, Verhütung, Erkennung oder zur Linderung von Krankheiten eingesetzt werden. Darunter fallen auch Diagnosemittel, medizinische Flüssigkeiten und Lösungen (Infusionen), homöopathische Mittel oder Arzneien, die in Apotheken zubereitet werden.
Wichtig zu wissen: Nicht zu Arzneimitteln zählen Lebensmittel, Nahrungsergänzungsmittel, Kosmetikprodukte, Tabakerzeugnisse, Biozide und Medizinprodukte.
Neben Arzneimitteln mit chemisch hergestellten Wirkstoffen gibt es auch pflanzliche Arzneimittel und die Gruppe der Biologika, die aus tierischen oder menschlichen Substanzen gewonnen werden.
Nicht nur die Entwicklung neuartiger Arzneimittel ist wichtig für das Gesundheitssystem, sondern auch Nachahmerprodukte (Generika). Sie kommen nach Ablauf des Unterlagen- und Patentschutzes auf den Markt.
Wofür werden Arzneimittel eingesetzt?
Arzneimittel sind sehr vielfältig und kommen für unterschiedliche medizinische Zwecke zum Einsatz:
- zur Verhütung von Erkrankungen: zum Beispiel Impfstoffe
- zur Heilung von Erkrankungen: zum Beispiel Antibiotika gegen bakterielle Infektionen
- zur Linderung von Beschwerden bei Erkrankungen: zum Beispiel fiebersenkende Mittel bei einem grippalen Infekt mit Fieber
- zur Diagnose von Erkrankungen: zum Beispiel Kontrastmittel bei einer Magnetresonanztomografie (MRT)
Manche Medikamente wie Antibiotika oder fiebersenkende Mittel nimmt man in der Regel nur kurzfristig für ein paar Tage ein. Sie helfen bei akuten Beschwerden wie Fieber oder unterstützen die Genesung bei akuten Erkrankungen wie bakteriellen Infektionen.
Andere Medikamente wie Diabetes-Medikamente oder Mittel gegen Bluthochdruck sind für die Langzeittherapie von chronischen Erkrankungen bestimmt und müssen regelmäßig über einen längeren Zeitraum oder sogar lebenslang eingenommen werden.
Wie bestimmte Medikamente richtig eingenommen und aufbewahrt werden, steht in der Packungsbeilage. Weitere Informationen zur Einnahme, Aufbewahrung und Entsorgung von Medikamenten erhalten Sie auch im Artikel Umgang mit Arzneimitteln.
Wo bekommt man Arzneimittel?
Die meisten Arzneimittel sind verschreibungspflichtig oder apothekenpflichtig. Verschreibungspflichtige Arzneimittel können nur mit einem ärztlichen Rezept in der Apotheke erworben werden. Apothekenpflichtige Arzneimittel kann man zwar ohne Rezept bekommen, allerdings nur in Apotheken.
Einige Medikamente dürfen außerhalb von Apotheken verkauft werden. Sie werden als freiverkäufliche Arzneimittel bezeichnet. Man kann sie zum Beispiel in Drogerien, Reformhäusern und Supermärkten kaufen. Voraussetzung für den Verkauf ist jedoch, dass die Händlerin oder der Händler die erforderliche Sachkenntnis nachweisen kann. So schreibt es das Arzneimittelgesetz vor (§ 50 AMG). Beispiele für freiverkäufliche Arzneimittel sind Arzneitees oder Lutschtabletten gegen Husten und Heiserkeit.
Mehr zum Verkauf von Arzneimitteln und zur Apothekenpflicht erfahren Sie im Artikel Rezeptpflichtige und rezeptfreie Arzneimittel.
Was sind pflanzliche Arzneimittel?
Unter pflanzlichen Arzneimitteln versteht man Medikamente, die als Wirkstoff ausschließlich pflanzliche Stoffe oder Zubereitungen oder Kombinationen daraus enthalten. Die Wirkstoffe werden also anders als bei vielen anderen Medikamenten nicht chemisch hergestellt, sondern aus Pflanzen gewonnen. Trotzdem können bei pflanzlichen Arzneimitteln Nebenwirkungen oder Wechselwirkungen mit anderen Medikamenten auftreten.
Darüber hinaus gibt es traditionelle pflanzliche Arzneimittel, die eine mehr als 30-jährige Tradition in der medizinischen Anwendung haben.
Was sind homöopathische Arzneimittel?
Homöopathische Arzneimittel sind Arzneimittel, die nach einem im Europäischen oder Homöopathischen Arzneibuch beschriebenen homöopathischen Zubereitungsverfahren hergestellt wurden. Sie können einen oder mehrere Ausgangsstoffe enthalten. Die Ausgangsstoffe werden nach im Arzneibuch festgelegten Regeln stark verdünnt. Dadurch soll die Wirkung verstärkt werden. Viele homöopathische Mittel sind so stark verdünnt, dass kein Ausgangsstoff mehr enthalten ist. Häufige Darreichungsformen homöopathischer Arzneimittel sind Streukügelchen (Globuli), Tropfen oder Tabletten.
Was sind Generika?
Wenn ein neuer Arzneiwirkstoff gefunden oder entwickelt wurde, lassen sich pharmazeutische Unternehmen diesen meist patentieren. Ein Patent gilt für 20 Jahre. Während dieser Zeit ist das Arzneimittel davor geschützt, von einem anderen Hersteller produziert und verkauft zu werden (Patentschutz). Somit kann das Medikament innerhalb dieser Zeit nur von dem Inhaber des Patents verkauft werden. Darüber hinaus dürfen die für die Zulassung eingereichten Daten zu klinischen Studien eine Zeitlang nicht für andere Zulassungen herangezogen werden (Unterlagenschutz).
Wenn der Unterlagen- und Patentschutz des Originalpräparates abgelaufen ist, können sogenannte „Generika“ nach vorheriger Zulassung in den Verkehr gebracht werden. Mitunter können Zulassungen auch schon vor Ablauf des Unterlagenschutzes erteilt werden. Generika sind Arzneimittel mit dem gleichen Wirkstoff, gleicher Darreichungsform, gleicher Wirkstärke und Dosierung sowie den gleichen Anwendungsgebieten. Für eine Zulassung muss das pharmazeutische Unternehmen nachweisen, dass das Generikum vergleichbar mit dem Originalpräparat ist. Zum Beispiel muss es vom Körper genauso aufgenommen und ausgeschieden werden.
Der Vorteil von generischen Arzneimitteln ist, dass sie deutlich kostengünstiger sind, da die Hersteller von Generika kein Geld in die klinische Forschung und Entwicklung investieren müssen. Generika schonen somit das Budget der Krankenkassen, die in der Regel einen Großteil der Kosten aller verschreibungspflichtigen Medikamente tragen.
Wichtig zu wissen: Generika sind genauso sicher und wirksam wie das Originalpräparat. Denn sie unterliegen der gleichen strengen Prüfung.
Was sind Biologika und Biosimilars?
Unter Biologika versteht man Medikamente, deren Wirkstoffe aus biologischen Substanzen wie Blut, Gewebe oder Zellen gewonnen werden. Sie enthalten zum Beispiel Proteine, Nukleinsäuren, Kohlenhydrate, Zellen oder Mikroorganismen. Dadurch weisen sie eine natürliche Veränderlichkeit auf – Fachleute sprechen von „Variabilität“ – und müssen besonders sorgfältig kontrolliert werden. Beispiele für Biologika sind Gerinnungsfaktoren, Antikörper und die meisten Impfstoffe.
Biosimilars sind Nachahmerprodukte von Biologika. Anders als Generika sind Biosimilars jedoch nicht identisch mit dem Wirkstoff des Originalpräparates, sondern nur sehr ähnlich, aber dennoch wirkungsgleich.
Wie werden Arzneimittel reguliert und zugelassen?
Die Sicherheit und die Wirksamkeit von Arzneimitteln müssen wissenschaftlich belegt werden, bevor sie auf den Markt kommen. Für eine Zulassung sind häufig klinische Studien notwendig, in denen die Wirksamkeit und Unbedenklichkeit des Arzneimittels an freiwilligen Testpersonen untersucht wird.
Bei vielen Arzneimitteln werden die gesammelten Studiendaten von nationalen Behörden wie dem Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) oder dem Paul-Ehrlich-Institut (PEI) geprüft.
Manche Arzneimittel werden von der europäischen Kommission zugelassen, koordiniert durch die Europäische Arzneimittelagentur (EMA). Dazu zählen unter anderem neue Wirkstoffe und Medikamente gegen bestimmte Erkrankungen wie Krebs oder in besonderen Verfahren hergestellte Arzneimittel.
Diese sind dann gleich für die ganze Europäische Union (EU) beziehungsweise den Europäischen Wirtschaftsraum zugelassen. Die Prüfung erfolgt hier ebenfalls durch Wissenschaftlerinnen und Wissenschaftler der nationalen Behörden. Diese Art der Zulassung wird auch als zentrales Zulassungsverfahren bezeichnet.
Die Zuständigkeit für die Überwachung der Arzneimittel nach ihrer Zulassung ist in Deutschland geteilt: Die Überwachung von Nebenwirkungen erfolgt durch die Bundesoberbehörden, also in Deutschland durch das BfArM und PEI. Für die übrige Überwachung – zum Beispiel die der Herstellung oder der Vermarktung – sind die Bundesländer zuständig.
Mehr darüber, wie Arzneimittel entwickelt, in Studien überprüft und zugelassen werden, lesen Sie im Artikel Zulassung von Arzneimitteln.
Registrierung statt Zulassung
Einen Sonderfall stellen homöopathische Arzneimittel ohne bestimmtes Anwendungsgebiet und traditionelle pflanzliche Arzneimittel dar: Für sie ist keine Zulassung nötig, eine Registrierung ist ausreichend. Dafür sind keine klinischen Studien nötig. Die Unbedenklichkeit der Arzneimittel muss aber trotzdem nachgewiesen werden.
Haben homöopathische Arzneimittel ein bestimmtes Anwendungsgebiet, zum Beispiel „fieberhafte Atemwegsinfekte“, müssen sie zugelassen sein – eine Registrierung reicht dann nicht aus.
Wo findet man weitere Informationen zu Arzneimitteln?
Vertiefende Informationen zu Arzneimitteln bietet das Bundesinstitut für Arzneimittel (BfArM) im Bürgerbereich seiner Website.
- Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM). Allgemeine Fragen. Aufgerufen am 24.04.2025.
- Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM). Arzneimittel. Aufgerufen am 24.04.2025.
- Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM). Homöopathische Arzneimittel. Aufgerufen am 24.04.2025.
- Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM). Zentralisiertes Verfahren. Aufgerufen am 24.04.2025.
- Bundesministerium für Gesundheit. Generika. Aufgerufen am 24.04.2025.
- Bundesministerium für Gesundheit. Zugang zu Arzneimitteln. Aufgerufen am 24.04.2025.
- Bundesministerium für Justiz. Gesetz über den Verkehr von Arzneimitteln (Arzneimittelgesetz). Stand: 23.10.2024.
- Gemeinsamer Bundesausschuss (G-BA). Biologika und Biosimilars: Austauschbarkeit von biotechnologisch hergestellten Arzneimitteln. Aufgerufen am 24.04.2025.
- Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG). gesundheitsinformation.de. Homöopathie. Aufgerufen am 24.04.2025.
- Paul-Ehrlich-Institut (PEI). Aufgaben. Aufgerufen am 24.04.2025.
In Zusammenarbeit mit dem Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM).
Stand:


